Tak salah bila dunia mendapuknya sebagai bapak ki mia modern. Ahli kimia Mus lim terkemuka di era kekhalifahan yang dikenal di dunia Barat dengan pang gilan Geber itu memang sangat fenomenal. Betapa tidak, 10 abad se be lum ahli kimia Barat bernama John Dal ton (1766-1844)? mencetuskan teori mo lekul kimia, Jabir Ibnu Hayyan (721M – 815 M) telah menemukannya di abad ke-8 M.Hebatnya lagi, penemuan dan eksperimennya yang telah berumur 13 abad itu ternyata hingga kini masih tetap dijadikan rujukan.?? Dedikasinya dalam pengembangan ilmu kimia sungguh tak ternilai harganya. Tak heran, jika ilmuwan yang juga ahli farmasi itu dinobatkan sebagai renaissance man (manusia yang mencerahkan).
Tanpa kontribusinya, boleh jadi ilmu kimia tak berkembang pesat seperti saat ini. Ilmu pengetahuan modern sungguh telah berutang budi kepada Jabir yang dikenal sebagai seorang sufi itu. Jabir telah menorehkan sederet karyanya dalam 200 kitab. Sebanyak 80 kitab yang ditulisnya itu mengkaji dan mengupas seluk-beluk ilmu kimia. Sebuah pencapaian yang terbilang amat prestisius.
Itulah sebabnya, ahli sejarah Barat, Philip K Hitti dalam History of the Arabs berujar, ?’Sesudah ilmu kedokteran, astronomi, dan matematika, bangsa Arab juga memberikan sumbangan yang begitu besar di bidang kimia.’? Penyataan Hitti itu merupakan sebuah pengakuan Barat terhadap pencapaian yang telah ditorehkan umat Islam di era keemasan.
Sejatinya, ilmuwan kebanggaan umat Islam itu bernama lengkap Abu Musa Jabir Ibnu Hayyan. Asal-usul kesukuan Jabir memang tak terungkap secara jelas. Satu versi menyebutkan, Jabir adalah seorang Arab. Namun, versi lain menyebutkan ahli kimia kesohor itu adalah orang Persia.? Kebanyakan literatur menulis bahwa Jabir terlahir di Tus, Khurasan, Iran pada 721 M.
Saat terlahir, wilayah Iran berada dalam kekuasaan Dinasti Umayyah. Sang ayah bernama Hayyan Al-Azdi, seorang ahli farmasi berasal dari suku Arab Azd. Pada era kekuasaan Daulah Umayyah, sang ayah hijrah dari Yaman ke Kufah, salah satu kota pusat gerakan Syiah di Irak. Sang ayah merupakan pendukung Abbasiyah yang turut serta menggulingkan Dinasti Umayyah.
Ketika melakukan pemberontakan, Hayyan tertangkap di Khurasan dan dihukum mati. Sepeninggal sang ayah, Jabir dan keluarganya kembali ke Yaman. Jabir kecil pun mulai mempelajari Alquran, matematika, serta ilmu lainnya dari seorang ilmuwan bernama Harbi Al-Himyari.
Setelah Abbasiyah menggulingkan kekuasaan Umayyah, Jabir memutuskan untuk kembali ke Kufah. Di kota Syiah itulah, Jabir belajar dan merintis karier. Ketertarikannya pada bidang kimia, boleh jadi lantaran profesi sang ayah sebagai peracik obat. Jabir pun memutuskan untuk terjun di bidang kimia.
Jabir yang tumbuh besar di pusat peradaban Islam klasik itu menimba ilmu dari seorang imam termasyhur bernama Imam Ja’far Shadiq. Selain itu, ia juga sempat belajar dari Pangeran Khalin Ibnu Yazid. Jabir memulai kariernya di bidang kedokteran setelah berguru pada Barmaki Vizier? pada masa kekhalifahan Abbasiyah berada dibawah kepemimpinan Harun Ar-Rasyid.
Sejak saat itulah, Jabir bekerja keras mengelaborasi kimia di sebuah laboratorium dengan serangkaian eksperimen. Dalam karirnya, ia pernah bekerja di laboratorium dekat Bawwabah di Damaskus. Salah satu ciri khasnya, ia mendasari? eksperimen-eksperimen yang dilakukannya secara kuantitatif. Selain itu, instrumen yang digunakan dibuat sendiri, menggunakan bahan berasal dari logam, tumbuhan, dan hewani. ?’Saya pertama kali mengetahuinya? dengan melalui tangan dan otak saya, dan saya menelitinya hingga sebenar
mungkin, dan saya mencari kesalahan yang mungkin masih terpendam.’? Kalimat itu kerap dituliskan Jabir saat mengakhiri uraian suatu eksperimen yang telah dilakukannya.
mungkin, dan saya mencari kesalahan yang mungkin masih terpendam.’? Kalimat itu kerap dituliskan Jabir saat mengakhiri uraian suatu eksperimen yang telah dilakukannya.
Setelah sempat berkarier di Damas – kus, Jabir pun dikabarkan kembali ke Kufah. Dua abad pasca-berpulangnya Jabir, dalam sebuah penggalian jalan telah ditemukan bekas laboratorium tempat sang ilmuwan berkarya. Dari tempat itu ditemukan peralatan kimianya yang hingga kini masih mempesona serta sebatang emas yang cukup berat.
Begitu banyak sumbangan yang telah dihasilkan Jabir bagi pengembangan kimia. Berkat jasa Jabir-lah, ilmu pengetahuan modern bisa mengenal asam klorida, asam nitrat, asam sitrat, asam asetat, tehnik distilasi, dan tehnik kristalisasi. Jabir pulalah yang menemukan larutan aqua regia (dengan menggabungkan asam klorida dan asam nitrat) untuk melarutkan emas.
Keberhasilan penting lainnya yang dicapai Jabir adalah kemampuannya mengapli kasi kan pengetahuan me? ngenai kimia ke dalam proses pembuatan besi dan logam lainnya, serta pencegahan karat. Ter nyata, Jabir jugalah yang kali pertama mengaplikasikan penggunaan mangan dioksida pada pembuatan gelas kaca.
Adalah Jabir pula yang pertama kali mencatat tentang? pemanasan anggur akan menimbulkan gas yang mudah terbakar. Hal inilah yang kemudian memberikan jalan bagi Al-Razi untuk menemukan etanol.
Selain itu, Jabir pun berhasil menyempurnakan proses dasar sublimasi, peng uapan, pencairan, kristalisasi, pembuatan
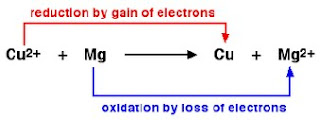
kapur, penyulingan, pencelupan, pemurnian, sematan (fixation), amalgamasi, dan oksidasi-reduksi. Apa yang dihasilkannya itu merupakan teknikteknik kimia modern.
kapur, penyulingan, pencelupan, pemurnian, sematan (fixation), amalgamasi, dan oksidasi-reduksi. Apa yang dihasilkannya itu merupakan teknikteknik kimia modern.
Tak heran, bila sosok dan pemikiran Jabir begitu berpengaruh bagi para ahli kimia Muslim lainnya seperti Al-Razi (9 M), Tughrai (12 M) dan Al-Iraqi (13 M). Tak cuma itu, buku-buku yang ditulisnya juga begitu besar pengaruhnya terhadap pengembangan ilmu kimia di Eropa. Jabir tutup usia pada tahun 815 M di Kufah.? heri ruslan (Republika)
===
Adikarya Sang Ilmuwan Besar
Dedikasi dan prestasi yang dicapai Jabir Ibnu Hayyan dalam bidang kimia terekam dengan baik lewat buku-buku yang ditulisnya. Tak kurang dari 200 buku berhasil ditulisnya.? Sebanyak 80 judul buku di antaranya mengupas hasil-hasil eksperimen kimia yang dilakukannya. Buku-buku itu sungguh amat berpengaruh hingga sekarang.Sebanyak 112 buku karya Jabir secara khusus ditulis untuk dipersembahkan kepada Barmakid?sang guru?yang juga pembantu atau wazir Khalifah Harun Ar- Rasyid. Buku-buku itu ditulis dalam bahasa Arab. Pada abad pertengahan, orang-orang Barat mulai menerjemahkan karya-karya Jabir itu ke dalam bahasa Latin (Tabula Smaragdina).Buku-buku itu lalu menjadi rujukan pada ahli kimia di Eropa.
Selain itu, sebanyak 70 buku karya Jabir lainnya juga? dialihbahasakan ke dalam bahasa Latin pada abad pertengahan. Dari ke-70 kitab berpengaruh itu, salah satu yang terkenal adalah Kitab Al-Zuhra yang diterjemakan menjadi Book of Venus, serta Kitab Al-Ahjar yang dialihbahasakan menjadi Book of Stones.
Sebanyak 10 buku yang ditulis Jabir lainnya adalah kitab pembetulan yang berisi penjelasan mengenai ahli kimia Yunani seperti Pythagoras, Socrates, Plato dan Aristoteles. Sisanya, kitab yang ditulis Jabir merupakan buku-buku keseimbangan. Dalam buku kelompok ini, Jabir melahirkan teori yang begitu terkenal, yakni ?teori keseimbangan alam.?
Risalat-risalat karya Jabir yang secara khusus membedah ilmu kimia antara lain? Kitab Al-Kimya dan Kitab Al-Sab?een. Kitab penting itu juga telah diterjemahkan ke dalam bahasa Latin di abad pertengahan. Kitab Al-Kimya menjadi sangat populer di Barat setelah diterjemahkan ke dalam bahasa Ingris oleh orang Inggris Robert of Chester pada 1144 M.
Al-Kimya versi alih bahasa berjudul ?The Book of Composition of Alchemy?. Sedangkan, Kitab Al-Sab?een diterjemahkan oleh Gerard of Cremona. Beberapa karya Jabir lainnya juga dialihbahasakan oleh Berthelot ke dalam bahasa Inggris antara lain; ?Book of Kingdom?, ?Book of the Balances?, serta ?Book of Eastern Mercur.?
Buku karya Jabir lainnya juga mendapat perhatian dari ilmuwan Inggris bernama Richard Russel. Pada abad ke-17 M, Russel menerjemahkan buku yang ditulis Jabir ke dalam bahasa Ingris berjudul ?Sum of Perfection?.
Dalam buku itu, Russel memperkenalkan Jabir dengan nama Geber?seorang pange? ran Arab terkenal yang juga seorang filsuf. ?Sum of Perfection? selama beberapa abad begitu populer dan berpengaruh. Buku itu telah mendorong terjadinya evolusi kimia modern. Begitu berpengaruhnya buku-buku karya Jabir di Eropa dan Barat umumnya telah dibuktikan dengan munculnya beberapa istilah teknis yang ditemukan dalam kamus kimia Barat dan menjadi kosa kata ilmia yang sebelumnya digunakan Jabir seperti istilah “alkali.” hri (Republika)
Forward from (Here)